Spin and spin-orbit interactions of electrons
上一节我们提到,根据斯特恩盖拉赫实验我们推出了原子具有(轨道)磁矩,那么理论上电子在磁场的作用下会发生能级分裂。其中由于磁量子数一共有
事实上仍有一些实验事实不符合上述规律,比如:
- 在非均匀磁场中一些处于S态的原子射线束,一束分裂为两束的现象.(按照上述理论,
,不应该分裂) - 氢原⼦巴尔末线系Hα 线是双线(如果光谱仪分辨本领更⾼,则是7条线)结构,与理论不符。
- 碱金属原子光谱是由更细的2或3条组成的,进一步分析表明,碱金属原子的能级具有双层结构,这直接导致了碱金属原子光谱精细结构的产生。
因此,一定存在一个未被考虑的磁矩——自旋。
自旋假设的提出
基态银原子(和铜一样,最外层仅有一个s电子)束通过不均匀磁场后分裂为两束,这要求2l+1为偶数,由于l为整数,因此实验结论违背了斯特恩-盖拉赫实验得出的结论。
对反常结果的分析:
- 对于基态s电子,由于发生了分裂,因此一定存在其他内源的磁矩,并且这个磁矩只有两个取向,且两个取向对称。
- 对于碱金属的双层结构可能是自旋磁矩导致能级裂分后,另一内源磁矩使裂分后的能级进一步裂分。
1925年,两位荷兰学生乌伦贝克和古兹密特在分析上述实验的基础上提出了大胆的看法:- 电子不是一个点粒子,它除了轨道角动量外,任何电子还都有相同的自旋角动量和自旋磁矩。
- 电子自旋角动量 S 的大小类似于“轨道”角动量,为
,s为自旋量子数。
仿照电子“轨道”角动量在外磁场方向上的分量取2l +1种, 电子自旋角动量在外磁场方向上的分量也只可能取 2s+1=2 种,即,其磁量子数为 .[1]
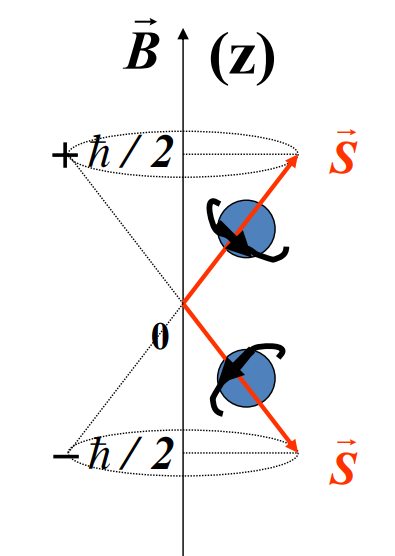
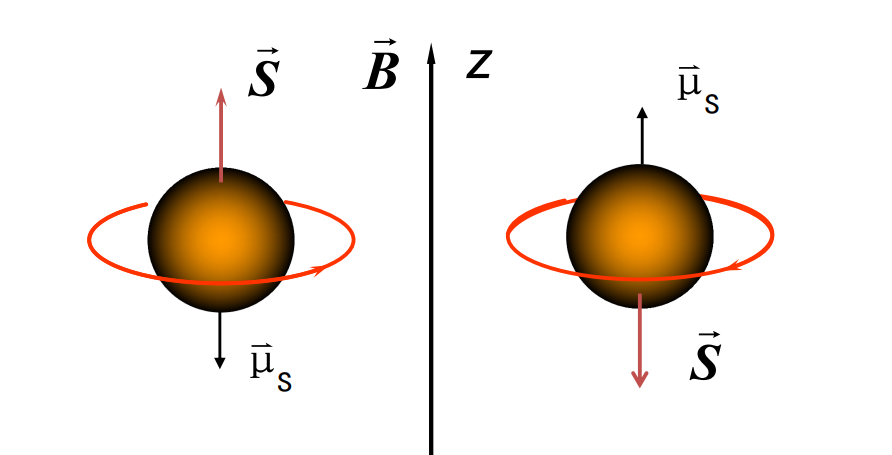
经典情况下(类比轨道磁矩的情况)
对于角动量j
这样一来,其对应的自旋磁矩为:
自旋假设成功解释了斯-盖实验(银原子)结果和一些基态s电子能级裂分的现象,但是其本身存在一些问题:
若把电子视为
电子自旋算符:
类比电子轨道角动量的算符:
然而角动量算符的本征函数是球谐函数,是分立的无限谱,自旋算符的本征值只有两个,其本征函数应是分立有限谱。
定义
其中:
则:
上面三个矩阵成为泡利矩阵,也满足自旋算符的对易关系。
自旋与轨道角动量耦合——总角动量
在磁场中,自旋角动量的取向只有两种:顺磁场和逆磁场。对于总角动量,其应为自旋角动量和轨道角动量之间的矢量和,且同样有:
设总角动量J是由两个子角动量
考虑到
于是:
因此
然而,若要计算总角动量对应的磁矩不能直接用角动量计算,而是需要一个朗德g因子,对于自旋和轨道角动量的磁矩来说:
因此以此类推[4],对于总角动量,其对应的磁矩为:
经过计算
上一节中我们在斯特恩-盖拉赫实验中得到了以下结果:
代入
从而我们得以从实验上求导对应朗德g因子。
然而上述讨论仅在外磁场不破坏s-l耦合时成立,并且仅考虑单个电子(在多电子原子中,原子实的自旋角动量和轨道角动量对原子整体没有贡献;对于另⼀些原⼦, 对原⼦的总⾓动量或总磁矩有贡献的电⼦不 ⽌⼀个, 但在⼤多数情况下,上式仍成⽴,只要把式中的 s, l 改为电⼦耦合成的总⾃旋S和总轨道⾓动量L即可)。
自旋与轨道角动量的作用
原子内的电子运动产生磁场与自旋产生的磁矩发生相互作用,常称为自旋
——轨道相互作用。
考虑磁场对能级的影响,由于电子有自旋磁矩
这就是由于自旋-轨道相互作用引起的附加能量,它能够使电子的能级裂分形成双层结构,特别的,由于s电子的l=0无,轨道角动量为零无轨道-自旋相互作用,因此附加能量为零,不发生能级裂分。
由毕奥-萨伐尔定律可以得到:
将其转化为以核为静止的坐标系:
同时,上述结论可以用狄拉克方程自动给出。